
来源:iNature
DEAD-box ATP依赖性解旋酶(DEAH / D)是主要参与基因表达调控和RNA加工的保守基因家族。 作为其原型,eIF4AI是蛋白质翻译起始复合物的必要组分。 利用基于野生型eIF4AI的筛选系统及其具有改变的接头结构域的L243G突变体,先前的研究发现了eIF4AI抑制剂sanguinarine(SAN)并用它来研究eIF4AI的催化机制。
2019年8月8日,复旦大学党永军,刘建伟及丁滪在Cell Chemical Biology 在线发表题为“Targeting the N Terminus of eIF4AI for Inhibition of Its Catalytic Recycling”的研究论文,该研究描述了eIF4AI-抑制剂复合物的晶体结构,并证明结合位点显示出某些特异性,这可以为靶向eIF4AI的药物设计提供基础。
另外,除竞争性抑制外,SAN的可能作用机制涉及通过阻碍eIF4AI的闭合构象的形成,来干扰eIF4AI催化循环过程。 此外,该研究结果突出了eIF4AI上新的靶向位点,并确认eIF4AI是一种可行的药理学靶标。

蛋白质合成是最重要的生物学功能之一,并受到严格的控制。在翻译(起始,延伸和终止)的三个主要步骤中,翻译起始是限速步骤。在启动期间,mRNA被募集到43S预启动复合物,其向mRNA扫描AUG起始密码子。eIF4AI / II促进了这种扫描过程,它可以解开和减轻mRNA的二级结构。

SAN是一种新型的eIF4AI抑制剂
真核翻译起始因子4AI(eIF4AI)是DEAD-box ATP依赖性解旋酶。在起始步骤中,eIF4AI解开mRNA的5'UTR中的二级结构并导致48S核糖体的形成。EIF4AI由N和C末端的两个刚性球形结构域组成,以及两者之间含有10个残基的柔性接头区域。eIF4AI解旋酶核心的打开和关闭由ATP结合和磷酸盐释放控制。RNA结合和ATP酶活性是DEAD-box解旋酶最重要的生化功能。一般而言,DEAD-box家族的所有成员都具有ATP酶和RNA解旋酶活性。除了eIF4AI之外,eIF4E(帽结合蛋白)和eIF4G(大支架蛋白)也是真核翻译起始的必要组分,并且与eIF4AI一起,这三种蛋白形成eIF4F复合物。
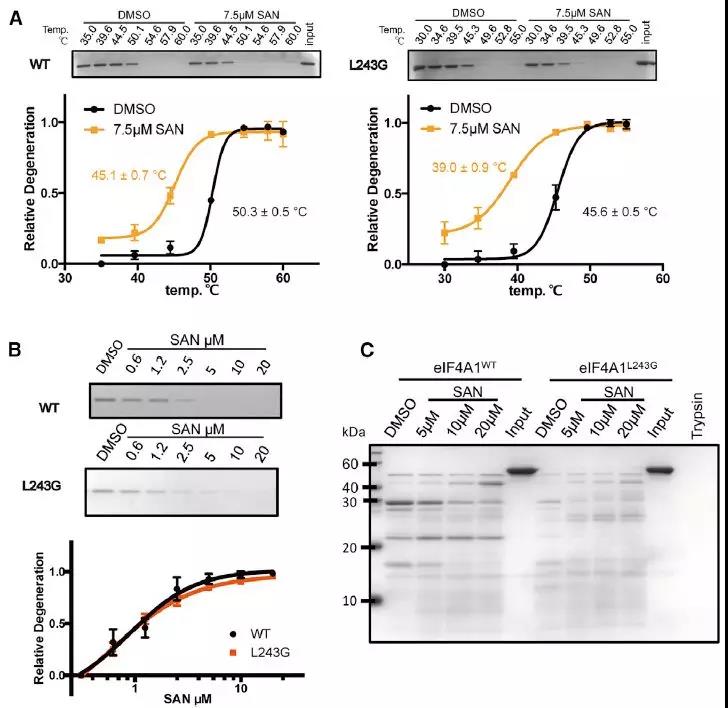
SAN直接体外结合eIF4AI
已经发现翻译起始因子,尤其是eIF4AI,与肿瘤发生和肿瘤进展密切相关,例如肝细胞癌,急性T细胞淋巴细胞白血病和黑素瘤(黑素瘤)。已经显示eIF4AI的表达与乳腺癌中的恶性程度和不良预后正相关。最近的研究表明,抑制eIF4AI特异性地下调许多癌基因和表观遗传因子的翻译,例如NOTCH1,MYC,MYB,ETS1,EZH2和MDM2。这些基因特别容易抑制eIF4AI的解旋酶活性,因为它会干扰5'UTRs中具有复杂结构的mRNA的表达。考虑到eIF4AI在翻译起始和致癌作用中的重要作用,该蛋白质正在成为抗肿瘤治疗的有希望的靶标。
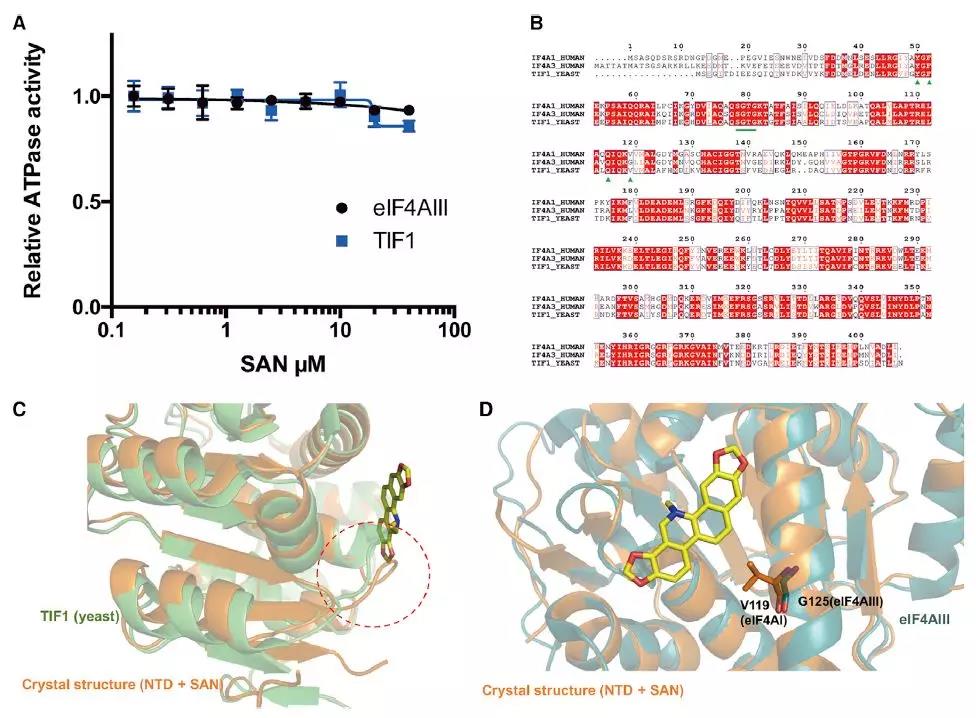
人eIF4AI,eIF4AIII和酵母TIF1的比对
针对eIF4AI被证明是一种有效的抗肿瘤方法。目前,主要有三种针对eIF4AI的小分子,均以天然产物为代表:silvestrol (rocaglate scaffold),hippuristanol和pateamine A(PatA)。silvestrol和PatA都是eIF4A酶活性的激活剂,但抑制翻译起始,只有hippuristanol抑制eIF4A的ATP酶和解旋酶活性。已证明Silvestrol和hippuristanol对多种多发性骨髓瘤(MM)细胞有效,并且CMLD010509(rocaglate)在MM的小鼠模型中显示出功效, PatA也证明在几种动物癌症模型中是有效的。最近,据报道,rocaglate A与eIF4A1和RNA形成的“双分子腔”结合。然而,PatA和马尿肼的精确结合位点以及分子作用机制仍然未知,这阻碍了这些分子的进一步优化和发展。

参考信息:
https://www.cell.com/cell-chemical-biology/fulltext/S2451-9456(19)30241-7
责任编辑:刘晔瀚





