
复旦大学基础医学院药理学系李洋课题组与中国科学院上海药物研究所柳红和周宇课题组深度合作揭示了一种溶酶体生成的调控新机制,阐明了多巴胺转运体在调控毒性蛋白降解过程中的新作用,并发现一类改善阿尔茨海默病 (Alzheimer’s disease, AD)的小分子化合物(LYsosome-Enhancing Compounds, LYECs),为临床改善AD提供了理论基础和潜在治疗靶标。该研究工作于2022年9月21日(世界阿尔茨海默病日)以Featured Article发表于阿尔茨海默病研究领域顶尖期刊Alzheimer's & Dementia。

溶酶体是细胞内负责物质降解的重要细胞器,其内部含有蛋白酶、脂酶等多种水解酶,可降解多种大分子物质,包括蛋白质和脂类等。溶酶体功能紊乱导致胞内物质不能被正常降解进而诱发多种重大疾病如神经退行性疾病。阿尔茨海默病 ( AD)是一种神经退行性疾病,其病理特征之一是脑部毒性蛋白Aβ的累积,进而导致神经元死亡和认知记忆等功能受损。因此,促进溶酶体生成,增强其降解Aβ淀粉样蛋白的功能,对改善AD具有意义。
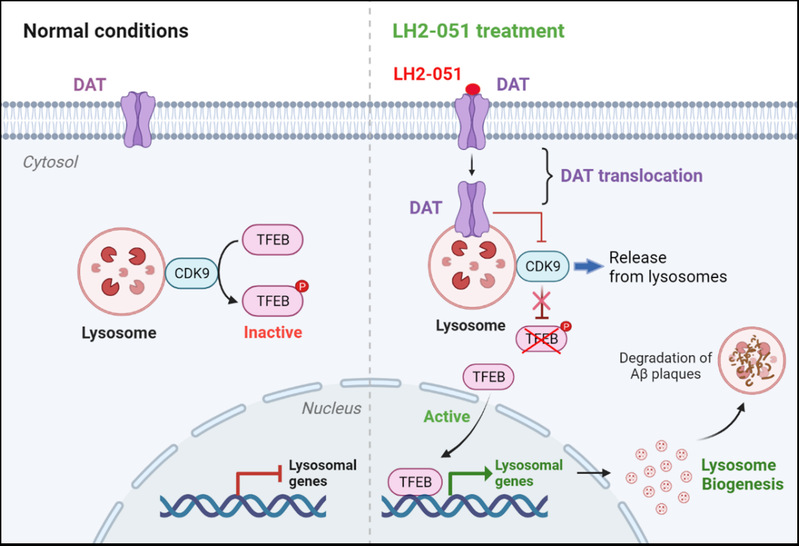
转录因子EB (Transcription factor EB, TFEB)是调控溶酶体生成的关键因子之一,研究表明通过激活TFEB可促进溶酶体和自噬相关基因的表达进而促进溶酶体的生成。我们自建高效稳定的系统,筛选出一系列促进溶酶体生成的小分子化合物LYECs。以LH2-051为代表的一类小分子化合物通过抑制多巴胺转运体(Dopamine transporter, DAT)促进溶酶体的生成。化合物LH2-051结合DAT后,诱导DAT从细胞膜转位至溶酶体膜上。随后溶酶体膜上的DAT调控周期蛋白依赖性激酶9(Cyclin-Dependent Kinase 9, CDK9)在溶酶体膜上的定位和活性,最终促进TFEB激活和溶酶体生成。在APP/PS1小鼠模型中发现LH2-051能显著促进小鼠大脑海马和皮层中溶酶体生成及Aβ42淀粉样蛋白的降解,进而改善小鼠行为学表现。
本工作依托复旦大学医学神经生物学国家重点实验室、中国科学院上海药物研究所新药研究国家重点实验室平台顺利开展。复旦大学基础医学院药理学系博士研究生尹利敏和中国科学院上海药物研究所-南京中医药大学联合培养博士研究生周建辉为本文共同第一作者。复旦大学基础医学院药理学系李洋青年研究员、中国科学院上海药物研究所柳红研究员和周宇研究员为本文的共同通讯作者。
Limin Yin*, Jianhui Zhou*, et al.,Yu Zhou#, Hong Liu#, and Yang Li#. Inhibition of the dopamine transporter promotes lysosome biogenesis and ameliorates Alzheimer’s disease–like symptoms in mice. Alzheimer’s& Dementia. 2022.https://doi.org/10.1002/alz.12776





