
RNA剪接失调在肿瘤发生发展中扮演关键角色,被认为是肿瘤的一个新分子特征和重要治疗靶标。肺癌是全球癌症导致死亡的首要原因,具有高度的异质性。尽管针对驱动突变的靶向治疗可显著改善患者生存,但治疗耐受和部分患者缺乏可靶向的驱动突变仍是临床上亟需解决的问题。小GTP酶RAC1在多种肿瘤中发生剪接改变,但其剪接亚型RAC1B与经典亚型RAC1A在肺癌中的功能差异及治疗前景尚不明确。近日,复旦大学基础医学院王勇波组与复旦大学附属肿瘤医院陈海泉组、中国科学院上海营养与健康研究所/南方科技大学王泽峰组、复旦大学基础医学院占昌友组合作,在Advanced Science在线发表了题为“Splicing Shift of RAC1 Accelerates Tumorigenesis and Defines a Potent Therapeutic Target in Lung Cancer”的研究。该研究揭示了RAC1剪接失调在肺腺癌中的促癌功能、机制与治疗意义,为肺癌提供了新的分子机制认识和治疗策略。

研究发现,RAC1B在肺腺癌患者中显著上调,尤其在EGFR突变患者中更为显著。在构建EGFR突变肺腺癌小鼠模型的基础上,通过肺敲除或过表达RAC1剪接亚型,揭示RAC1B而非RAC1A亚型促进肺腺癌细胞增殖与肿瘤生长。机制研究表明,RAC1B通过特异性结合鸟嘌呤核苷酸交换因子GDS1而被激活,进而抑制EGFR的溶酶体转运和降解,维持EGFR蛋白稳定性。剪接调控因子系统鉴定发现剪接因子RBM10抑制RAC1B剪接。基于肺腺癌患者来源类器官和移植瘤模型及脂质体纳米颗粒包裹的siRNA治疗实验表明,靶向抑制RAC1B可显著抑制肿瘤生长,并增强EGFR抑制剂的治疗效果。本研究系统阐明了RAC1剪接亚型在肺癌中的功能差异及分子机制,提出靶向RAC1B的治疗方法,为肺腺癌精准治疗提供了新方向(图1)。
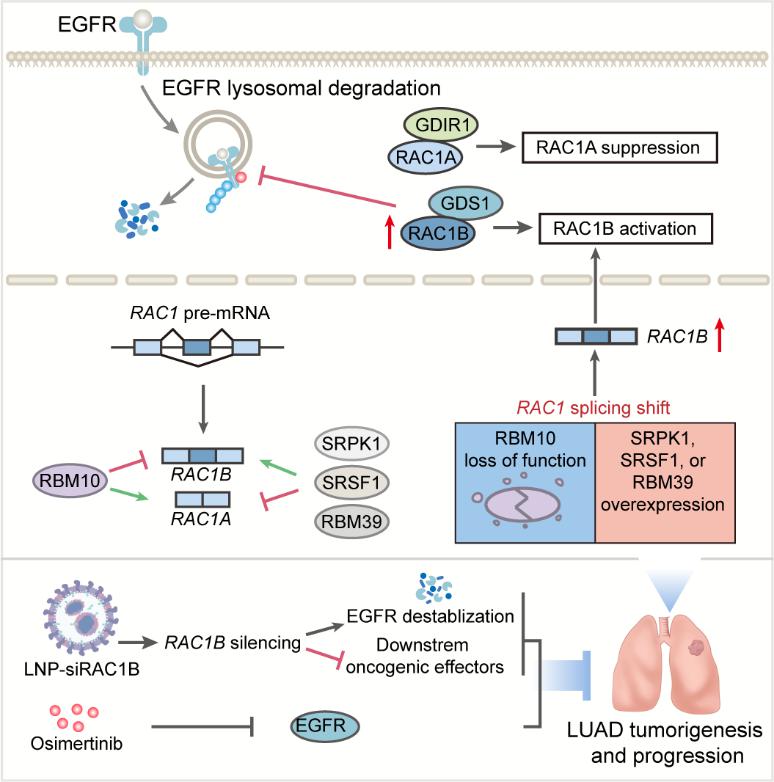
图1 肺腺癌中RAC1剪接失调的促癌功能、分子机制与治疗意义
复旦大学基础医学院王勇波、复旦大学附属肿瘤医院陈海泉、南方科技大学王泽峰以及复旦大学基础医学院占昌友为本文的共同通讯作者,复旦大学附属肿瘤医院博士生阎越人(已毕业)、中国科学院上海营养与健康研究所博士生王宁(已毕业,现为华盛顿大学博士后)为共同第一作者。本研究受到国家自然科学基金、上海市自然科学基金等项目支持;得到了中国科学院分子细胞科学卓越创新中心/西湖大学季红斌教授、复旦基础医学院细胞与遗传医学系、复旦大学附属肿瘤医院胸外科团队的大力支持。
原文链接:http://doi.org/10.1002/advs.202503322





